Семаглутид – Лекарство за Отслабване – Ефективност и Рискове Според Клиничните Данни
Прескочи до:
Семаглутид е едно от най-изследваните лекарства в своя клас и неговите клинични програми – SUSTAIN, PIONEER, STEP, OASIS, ESSENCE и SELECT – включват десетки хиляди пациенти по целия свят.
Това е лекарствено вещество от класа на инкретиновите миметици и по-конкретно агонистите на рецептора на глюкагоноподобния пептид-1 (GLP-1), разработено от датската компания Novo Nordisk.
Предлага се под три търговски наименования, които представляват следното:
- Писалка семаглутид в дози до 1мг (подкожна инжекция за лечение на захарен диабет тип 2)
- Таблетки семаглутид в дози до 14мг (орална таблетка за захарен диабет тип 2).
- Писалка семаглутид в дози до 2.4мг (подкожна инжекция, а вече и орални таблетки за лечение на затлъстяване)
Медикаменти които гарантирано съдържат семаглутид, могат да бъдат набавени САМО от аптечната мрежа, след като получите електронна рецепта от квалифициран лекар,
Какво Представлява Семаглутид?
Семаглутид е синтетичен аналог на човешкия глюкагоно-подобен пептид-1 (GLP-1) – хормон, секретиран от L-клетките на тънкото черво в отговор на прием на храна.
Одобрен е от Американската агенция по храните и лекарствата (FDA) и Европейската агенция по лекарствата (ЕАЛ) за:
- лечение на захарен диабет тип 2
- хронично управление на теглото при наднормено тегло и затлъстяване
- за намаляване на сърдечносъдови инциденти при пациенти с наднормено тегло или затлъстяване и установено сърдечносъдово заболяване
- за лечение на чернодробна фиброза при метаболитно-асоцииран стеатохепатит (MASH)
Молекулата се състои от 31 аминокиселини и притежава 94% еднаква структура с естествения човешки GLP-1 който се продуцира след хранене [1],[2].
6-те процента разлика идват от две основни модификации:
- На позиция 8 аланинът е заменен с алфа-аминоизомаслена киселина (Aib), което прави молекулата устойчива на разграждане от ензима дипептидил пептидаза-4 (DPP-4). Нативният GLP-1 се разгражда от DPP-4 за по-малко от 2 минути, докато семаглутид е напълно резистентен към това разграждане [3].
- Към лизина на позиция 26 е прикрепена C18 мастна диациделна верига посредством линкер. Тази мастна верига позволява на семаглутид да се свърже нековалентно с албумина в кръвната плазма, което значително забавя неговото бъбречно елиминиране и протеолитично разграждане [3].
В резултат на тези структурни модификации полуживотът на семаглутид е приблизително 7 дни, което позволява приложение веднъж седмично [1].
Това позволява и постигане на стабилни плазмени концентрации при приложение веднъж седмично, без значителни пикове и спадове, каквито се наблюдават при ежедневно приложение на по-краткодействащи агенти [3].
Механизъм на Действие на Семаглутид
Семаглутид действа чрез свързване и активиране на GLP-1 рецепторите, намиращи се в панкреаса, мозъка, сърцето, черния дроб, бъбреците и стомашно-чревния тракт. Основните му ефекти включват [1],[4]:
- Стимулиране на секрецията на инсулин от бета-клетките на панкреаса по глюкозозависим начин — инсулинът се освобождава само при повишени нива на кръвната захар, което минимизира риска от хипогликемия.
- Потискане на секрецията на глюкагон от алфа-клетките на панкреаса, намалявайки хепаталната глюкозна продукция.
- Забавяне на стомашното изпразване, което намалява постпрандиалните пикове на кръвна захар и допринася за усещане за ситост.
- Действие върху хипоталамуса и мозъчния ствол — семаглутид преминава кръвно-мозъчната бариера и се свързва с GLP-1 рецептори в хипоталамуса (ядро аркуатум) и в area postrema, намалявайки желанието за храна, физиологичния и хедонистичния апетит и енергийния прием.
- Кардиопротективни ефекти — намалява оксидативния стрес, атеросклеротичното възпаление и има директни ефекти върху миокарда и ендотела, независимо от гликемичния контрол.
За Какво е Ефективен и Одобрен Семаглутид?
Програмата SUSTAIN – лечение на ДТ2
Първоначално, Семаглутид е изследван за лечение на захарен диабет тип 2 в клинична програма SUSTAIN (SUSTAIN 1-7), включваща над 7000 пациенти в множество рандомизирани клинични проучвания [5].
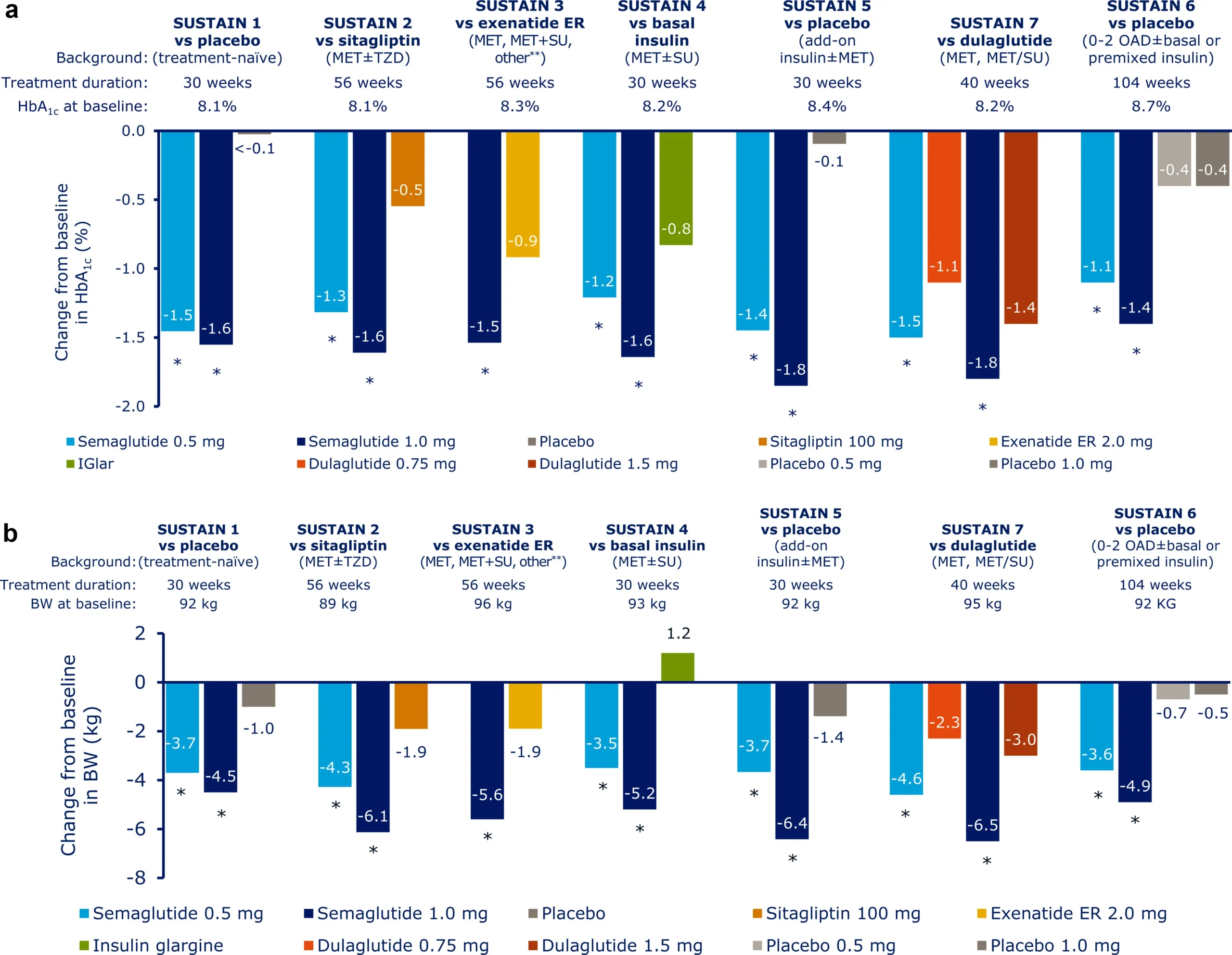
Основните резултати от тези проучвания са свързани с контрола над кръвната захар измерен чрез гликирания хемоглобин (HbA1c), и показват следното:
- Редукция на HbA1c: семаглутид в доза 1мг/седмица намалява HbA1c средно с 1.3-1.8% пункта спрямо изходното ниво в различните проучвания.
- Загуба на тегло: -3.6-6.5 кг при доза 1мг/седмица.
- Директни сравнения с други препарати в програмата SUSTAIN показват, че семаглутид 1мг/седмица превъзхожда ситаглиптин (DPP-4 инхибитор), други GLP-1 агонисти (екзенатид и дулаглутид), и инсулин по отношение на редукцията на HbA1c.
В 40-седмично проучване включващо семаглутид в доза 2мг/седмица, участниците с ДТ2 губят средно по почти 7 кг при усредненно начално тегло около 100кг и имат допълнителни подобрения на контрола над кръвната захар [6].
Това води до одобрението на семаглутид в дози до 2мг/седмица за лечение на ДТ2.
SUSTAIN-6 – сърдечно-съдови ползи при диабет тип 2
Едно от проучванията в тази програма е проучването SUSTAIN-6, което е рандомизирано двойно-сляпо контролирано проучване включващо 3297 пациенти с диабет тип 2 и висок сърдечно-съдов риск, които са проследявани в продължение на 104 седмици [7].
Участниците са рандомизирани да получават семаглутид 0.5 мг/седмица, 1мг/седмица или плацебо. Основните резултати според проучването са:
- Риска от смърт от сърдечносъдови причини, нефатален миокарден инфаркт или нефатален инсулт (MACE) е едва 6.6% в групата на семаглутид спрямо 8.9% при плацебо (около 26% по-нисък относителен риск).
- Най-значимо е намален относителния риск от инсулт с около 39%.
- Това води до одобрението на семаглутид за редукция на сърдечно съдовия риск при пациенти с ДТ2.
Важно предупреждение е че в SUSTAIN-6 се наблюдава значимо по-висока честота на бърза прогресия на диабетната ретинопатия при пациентите, лекувани с семаглутид.
Счита се, че това може да е свързано с твърде бързото подобряване на гликемичния контрол при пациенти с предшестваща ретинопатия. Затова при пациенти с диабетна ретинопатия е препоръчителен офталмологичен мониторинг.
FLOW – бъбречни ползи при диабет тип 2
Проучването FLOW (Flow in Renal Outcomes With Semaglutide) изследва ефекта на семаглутид при пациенти с хронично бъбречно заболяване (ХБЗ) и захарен диабет тип 2 [8].
Данните за бъбречните резултати показват:
- 24% намаление на риска от първичния бъбречен краен показател (HR 0.76; 95% ДИ 0.66-0.88; P=0.0003), включващ значително влошаване на бъбречната функция, бъбречна заместителна терапия или смърт от бъбречни или сърдечно-съдови причини.
- 29% по-нисък риск от смърт от сърдечносъдови причини.
Тези резултати са значими за огромна популация пациенти с напреднал диабет тип 2, тъй като при тях бъбречното влошаване представлява водеща причина за заболеваемост и смъртност [8].
Програмата PIONEER – перорален семаглутид за лечение на ДТ2
Освен като инжекции, семаглутид е ефективен и в перорална форма. Това е значителен пробив, тъй като пептидните молекули традиционно не се абсорбират достатъчно след перорален прием.
Клиничната програма PIONEER (PIONEER 1-8) е тази която оценява ефикасността и безопасността на семаглутид като първия перорален GLP-1 рецепторен агонист [9].
Проучванията обхващат различни групи пациенти със захарен диабет тип 2 и го сравняват с плацебо и основни конкурентни терапии.
Ключовите резултати от програмата показват:
- Редукция на HbA1c: Оралният семаглутид (в дози до 14мг/ден) осигурява понижение на HbA1c средно с 1 до 1.5 процентни пункта, превъзхождайки значително плацебо, емпаглифлозин (SGLT2 инхибитор) и ситаглиптин (DPP-4 инхибитор).
- Загуба на тегло: Пациентите губят средно между 2.2 и 5.0 кг, като редукцията е по-отчетлива в сравнение с емпаглифлозин и ситаглиптин.
- Сравнение с инжекционен GLP-1 RA: В проучването PIONEER 4 оралният семаглутид (14 мг/ден) демонстрира сходна ефективност спрямо инжекционния лираглутид (1.8 мг/ден) по отношение на гликемичния контрол, и дори води до по-голяма загуба на тегло.
- Приложение при напреднал диабет: При пациенти на инсулинова терапия (PIONEER 8) или с бъбречно увреждане (PIONEER 5), медикаментът успешно понижава кръвната захар и теглото, като дори позволява намаляване на общата дневна доза инсулин, намалявайки риска от хипогликемии.
Резултатите от PIONEER категорично доказват, че пероралният семаглутид предоставя ефикасност, сравнима с тази на инжекционните препарати, при запазен профил на безопасност.
Това го прави отлична алтернатива за пациенти, които се нуждаят от това лечение, но предпочитат таблетна форма пред инжекции.
SOUL – сърдечно-съдови ползи при диабет с перорален семаглутид
Проучването SOUL (Semaglutide cardiOvascular oUtcomes triaL) е специално проектирано за оценка на сърдечно-съдовата ефикасност на оралния семаглутид (14 mg/ден) при пациенти с диабет тип 2 и установена атеросклероза и/или хронично бъбречно заболяване.
Резултатите са публикувани в New England Journal of Medicine през март 2025 г. [10].
Проучването включва:
- Общо 9650 участници на възраст ≥50 г. с диабет тип 2 и HbA1c 6.5-10%, с поне едно от: коронарна болест, цереброваскуларна болест, симптоматична периферна артериална болест или хронично бъбречно заболяване.
- Рандомизирани 1:1 на орален семаглутид 14 mg/ден или плацебо.
- Медианно проследяване от около 49.5 месеца (около 4 години).
Резултати:
- Риска от смърт от сърдечносъдови причини, нефатален миокарден инфаркт или нефатален инсулт (MACE) е 12.0% в групата на семаглутид (579/4825) спрямо 13.8% при плацебо (668/4825) което е равносилно на 14% относително намаление на риска.
- Сериозните нежелани реакции са 47.9% при семаглутид спрямо 50.3% при плацебо — т.е. по-малко при лечението.
- Стомашно-чревни нарушения: 5.0% при семаглутид спрямо 4.4% при плацебо.
SOUL е важно допълнение към съществуващите данни, тъй като потвърждава, че сърдечносъдовата полза от GLP-1 рецепторните агонисти е приложима и за оралната форма на семаглутид — не само за инжекционната. Това е значимо клинично откритие, тъй като пероралното приложение е предпочитано от много пациенти [10].
Програмата STEP – лечение на затлъстяване чрез семаглутид като инжекция за отслабване
Медикаментът за отслабване съдържащ семаглутид е одобрен на базата на данните от клиничната програма STEP.
Тя предоставя мащабни и категорични доказателства за ефикасността на инжекционния семаглутид в доза от 2.4 мг/седмично при медикаментозното лечение на затлъстяване, съчетано с промени в начина на живот.
Ключовите резултати от отделните проучвания ясно очертават профила на медикамента и ефективността при дългосрочна терапия:
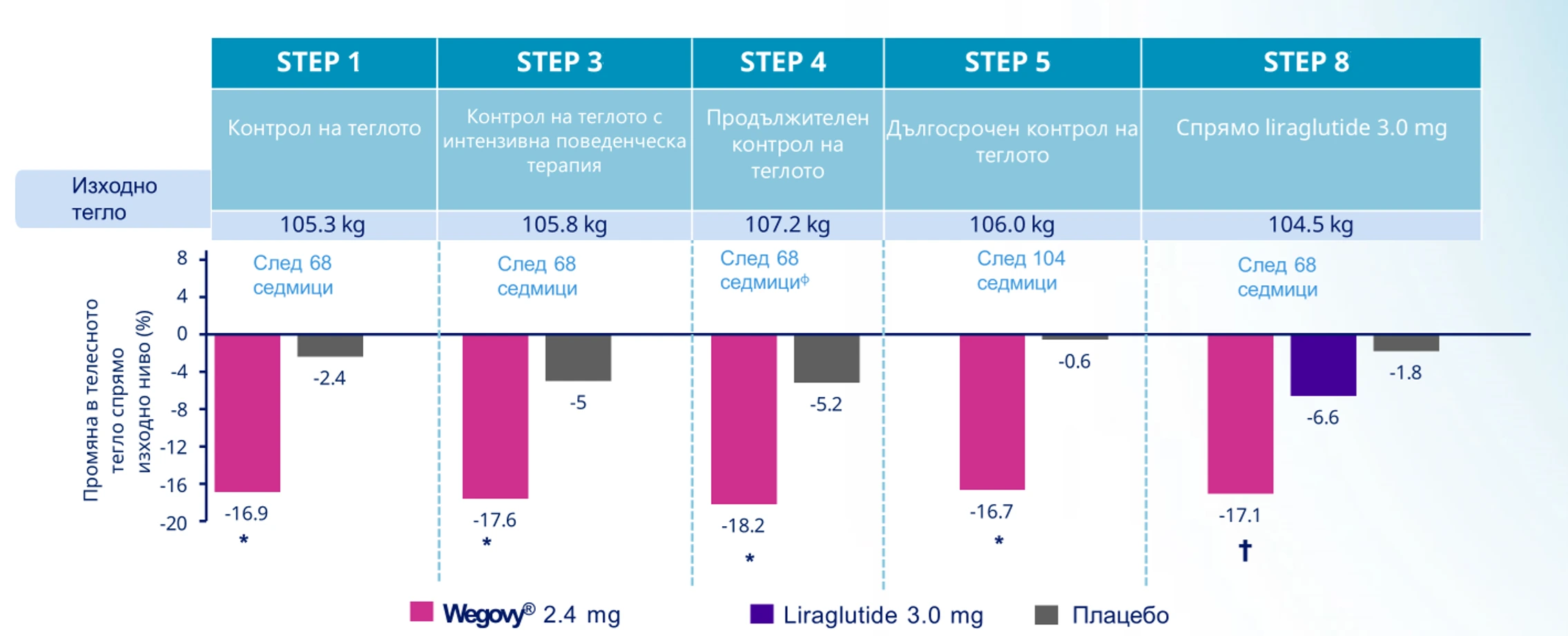
- STEP 1 (Пациенти без диабет): Проучването обхваща 1961 възрастни с ИТМ ≥30 kg/m2 или ≥27 kg/m2 и придружаващо заболяване. За 68 седмици семаглутид води до средна редукция на теглото от −14.9% (−15.3 кг) спрямо −2.4% при плацебо, като 86.4% от лекуваните губят поне 5% от теглото си, а 50.5% постигат над 15% редукция спрямо началното тегло [11].
- STEP 2 (Пациенти с диабет тип 2): При 1210 участници със специфичен метаболитен профил ефективността остава висока, макар и очаквано по-умерена спрямо тези без диабет. Отчита се средна редукция от −9.6% в сравнение с −3.4% при плацебо, като 68.8% от пациентите на семаглутид постигат ≥5% загуба на тегло спрямо 28.5% от контролната група [12].
- STEP 4 (Поддържане на теглото): Изследва ефекта от спиране на лечението след първоначален 20-седмичен период със средна загуба на тегло от −10.6%. Пациентите, преминали на плацебо след този период, бързо наддават с +6.9%, докато продължилите приема на семаглутид постигат допълнителна редукция от −7.9% за обща загуба от −17.4%, което е свързано с хроничния характер на затлъстяването и нуждата от постоянно лечение [13].
- STEP 5 (Дългосрочна ефикасност за две години): Проучването проследява 304 пациенти в продължение на 104 седмици. Резултатите показват, че постигнатата през първата година редукция се запазва стабилно, завършвайки със среден спад от −15.2% спрямо −2.6% при плацебо, което категорично потвърждава дългосрочните ползи от непрекъснатата употреба на медикамента [14].
Програмата OASIS — Орален Семаглутид като хапчета за Отслабване
Паралелно с програмата STEP, Novo Nordisk провежда клиничната програма OASIS (Oral Semaglutide Treatment Effect in People with Obesity), изследваща ефикасността на пероралния семаглутид при по-висока доза от 50 mg/ден за лечение на затлъстяване.
OASIS 1 е основното проучване, което е публикувано в The Lancet и включва 667 възрастни с BMI ≥30 kg/m² или ≥27 kg/m² с поне едно свързано с теглото заболяване, но без захарен диабет.
Участниците са рандомизирани 1:1 на орален семаглутид, ескалиран до 50 мг/ден, или плацебо в продължение на 68 седмици [15].
Резултатите:
- Средна редукция на теглото: -15.1% при орален семаглутид 50 mg спрямо -2.4% при плацебо (разлика -12.7 процентни пункта; 95% ДИ -14.2 до -11.3; P<0.0001).
- 85% от участниците постигат ≥5% редукция спрямо 26% при плацебо.
- 69% постигат ≥10% редукция спрямо 12% при плацебо.
- 54% постигат ≥15% редукция спрямо 6% при плацебо.
- 34% постигат ≥20% редукция спрямо 3% при плацебо.
Особено забележително е, че оралният семаглутид 50 mg/ден постига сравнима ефикасност с инжекционния семаглутид 2.4 mg/седмично — резултатите от OASIS 1 са практически много близки с тези от STEP 1, въпреки принципно различния начин на приложение.
Стомашно-чревните нежелани реакции са по-чести (80% при активното лечение), но предимно леки до умерено тежки.
По-скорошното проучване OASIS 4 е това което изследва по-ниска доза от 25 mg/ден орален семаглутид при 307 участника без диабет в продължение на 64 седмици [16].
Резултатите показват средна редукция на теглото от -13.6% спрямо -2.2% при плацебо. Това е отново клинично значим резултат, но 25мг/ден се оказва и по-поносима доза спрямо 50мг/ден.
Поради тази причина, семаглутид таблетки са одобрени за лечение на затлъстяването в дози до 25мг/ден.
SELECT – Сърдечносъдови ползи при Затлъстяване БЕЗ Диабет
Проучването SELECT (Semaglutide Effects on Cardiovascular Outcomes in People with Overweight or Obesity) е първото в света проучване, демонстрирало, че GLP-1 рецепторен агонист намалява сърдечносъдовия риск при пациенти с наднормено тегло или затлъстяване, но БЕЗ захарен диабет [17].
Характеристики на проучването:
- Общо 17 604 участници с установено сърдечносъдово заболяване и ИТМ над 27 кг/м², но без диабет.
- Участниците са рандомизирани да получават семаглутид 2.4 мг/седмица подкожно или плацебо.
- Средното проследяване е 39.8 месеца.
Резултати:
- Първичен краен показател (MACE): 6.5% в групата на семаглутид спрямо 8.0% при плацебо което е равно на – 20% относително намаление на риска.
- Смъртност от всякаква причина -19% относително намаление на риска.
- Сърдечна недостатъчност -18% относително намаление на риска.
Тези резултати означават, че семаглутид намалява сърдечно-съдовата смъртност не само чрез подобряване на гликемичния контрол (тъй като пациентите нямат диабет).
Вместо това, най-вероятно той оказва положителен ефект чрез механизми, свързани с противовъзпалителни ефекти, намаляване на теглото, подобряване на артериалното налягане и директни кардиопротективни ефекти на GLP-1 рецепторната активация [17].
По тази причина, семаглутид е първия медикамент за отслабване който е одобрен и за редукция на риска от сърдечно съдови заболявания.
Essense – Семаглутид за лечение на омазнен черен дроб и стеатохепатит с фиброза
ESSENCE е международно, многоцентрово, двойно-сляпо, плацебо-контролирано проучване, в което 1197 пациенти с биопсично доказан стеатохепатит (MASH) и фиброза стадий 2 или 3 са рандомизирани 2:1 към семаглутид 2.4 мг подкожно веднъж седмично или плацебо за 240 седмици [18].
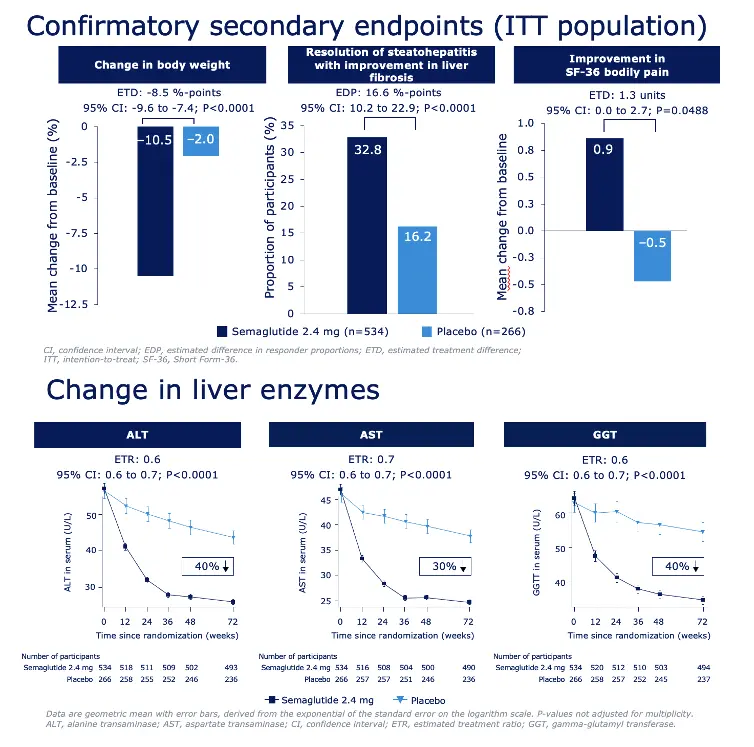
Според текущите данни от първите 800 пациенти, 72 седмици на терапия са постигнали резолюция на стеатохепатита без влошаване на фиброзата при 62.9% от пациентите на семаглутид срещу 34.3% при плацебо.
Редукция на чернодробната фиброза без влошаване на стеатохепатита е регистрирана при 36.8% срещу 22.4% при плацебо.
Комбинираният резултат – едновременна резолюция на стеатохепатита и подобрение на фиброзата – е постигнат при 32.7% срещу едва 16.1% при плацебо.
Средната загуба на тегло е -10.5% при семаглутид срещу -2.0% при плацебо.
По тази причина, на 15 август 2025 г. FDA одобри семаглутид за лечение на възрастни с умерена до напреднала чернодробна фиброза (стадий F2–F3), превръщайки го в втората одобрена терапия за стеатохепатит след медикамента resmetirom.
Резултатите от втората част на ESSENCE, която ще проследи клинични крайни точки като смъртност, чернодробна трансплантация и цироза, предстоят и ще изяснят дали хистологичното подобрение се транслира в реална клинична полза на дългосрочен план.
Как Се Дозира Семаглутид?
Дозирането на семаглутид следва принципа на постепенно нагласяне (titration), при което дозата се увеличава бавно, за да се минимизират стомашно-чревните нежелани реакции. Начинът на дозиране зависи от показанието и продукта.
Семаглутид за захарен диабет тип 2
Този вид семаглутид се прилага подкожно веднъж седмично в един и същи ден от седмицата:
- 0.25 mg веднъж седмично в продължение на 4 седмици.
- 0.5 mg веднъж седмично в продължение на минимум 4 седмици.
- При необходимост от по-добър гликемичен контрол: увеличение до 1.0 mg веднъж седмично за продължително лечение.
- Максималната одобрена доза от ЕАЛ е 2.0 mg веднъж седмично, но тя не е налична в България.
Всяка една от тези дози може да бъде поддържаща доза, в зависимост от ефекта на медикамента.
Перорален семаглутид за захарен диабет тип 2
Много е важно медикамента да се приема сутрин на гладно и с МАЛКО количество вода (до 100 мл), поне 30 минути преди пръв прием на храна, напитки или други лекарства.
Схемата за дозиране е:
- 3 mg веднъж дневно × 30 дни.
- 7 mg веднъж дневно за поне 30 дни или продължително лечение.
- При необходимост от по-добър контрол: 14 mg веднъж дневно.
Отново, всяка една от тези дози може да бъде поддържаща доза, в зависимост от ефекта на медикамента.
Семаглутид инжекции за управление на теглото
Семаглутид се прилага подкожно веднъж седмично по схема на постепенно нагласяне:
- 0.25 mg/седмица × 4 седмици
- 0.5 mg/седмица × 4 седмици
- 1.0 mg/седмица × 4 седмици
- 1.7 mg/седмица × 4 седмици
- 2.4 mg/седмица (поддържаща доза)
Целият диапазон от дози на семаглутид за отслабване е наличен в България. Отново, всяка една от тези дози може да бъде поддържаща доза, в зависимост от ефекта на медикамента.
Семаглутид таблетки за управление на теглото

Отново, всяка една от тези дози може да бъде поддържаща доза, в зависимост от ефекта на медикамента.
Този медикамент не е наличен в България към момента.
Нежелани Реакции и Безопасност
Семаглутид е добре проучен по отношение на безопасността в многобройни мащабни клинични изпитвания. Нежеланите реакции са предимно стомашно-чревни и са по-изразени в самото начало на терапията [19].
Най-Чести Нежелани Реакции
Данните от програмите STEP и OASIS прилагащи семаглутид в най-високи дози показват сходни честоти.
По-конкретно, данните от проучването STEP 1 с инжекционен семаглутид в доза 2.4/седмица показват следните честоти на нежелани реакции [11]:
- Гадене: ~44%
- Диария: ~30%
- Повръщане: ~24%
- Констипация (запек): ~24%
Честотата на прекратяване на лечението поради нежелани реакции в STEP 1 е ~7% в групата на семаглутид спрямо ~3% при плацебо.
Важно е да се отбележи, че стомашно-чревните нежелани реакции са предимно преходни и намаляват след стабилизиране на дозата.
Те са дозозависими и именно затова бавното ескалиране на дозата (на всеки 4 седмици или дори повече) е от съществено значение [19].
Въз основа на данните от клиничното проучване OASIS 1 (перорален семаглутид 50 mg/дневно), честотата на най-разпространените странични ефекти е следната [15]:
- Гадене: ~42%
- Констипация (запек): ~26%
- Диария: ~22%
- Повръщане: ~18%
Общо около 80% от пациентите на активно лечение съобщават за поне една стомашно-чревна нежелана реакция (спрямо 46% в плацебо групата), но в огромното си мнозинство тези оплаквания са леки до умерени и се проявяват предимно в периода на повишаване на дозата.
Редки но Сериозни Нежелани Реакции (Редки)
Панкреатит и холелитиаза
- Риска е реален особено в началото на терапията. Панкреатит е регистриран в клиничните проучвания с честота около 0.1-0.3%, a жлъчните камъни са по-чести – при около 1-3% от пациентите.
- Тези странични ефекти възникват при значителна и рязка редукция на тегло – черният дроб отделя повишено количество холестерол в жлъчката, което насърчава образуването на утайка и/или камъни. Камъните възпаляват мехура, а утайката може да допринесе за възпаление на панкреаса. Тези странични ефекти се наблюдават при рязко отслабване по всякакви причини, вкл. поради краш диета или бариатрична хирургия. Възможно е и забавяне на перисталтиката от самия медикамент.
- За ефективна превенция, терапията трябва да се проследи от лекар, който да проследява прогреса ежеседмично през първите няколко седмици, когато отслабването е най-бързо. Да се титрира дозата така че да се поддържа в началото темп около 1% загуба на тегло на седмица.
- Важно е и поддържане на адекватен прием на мазнини (около 20-25 г на хранене), тъй като пълното им изключване допълнително потиска жлъчната моторика.
Дехидратация
- Медикамента потиска не само желанието за храна, но и за течности. Това може да доведе до дехидратация, особено в случаи съчетани с повръщане или диария. Острата дехидратация носи и риск за остро бъбречно увреждане при пациенти с хронични заболявания и напреднала възраст.
Загуба на Мускулна Маса
- Значителна загуба на тегло при всеки метод е свързана с известна загуба на мускулна маса. Препоръчва се съчетаване на лечението с протеинова диета (1.2-1.6 g протеин/kg тегло) и редовни упражнения с тежести за запазване на мускулния тонус.
Предупреждения и Противопоказания за Семаглутид
- Тироидни C-клетъчни тумори: при лабораторни животни (гризачи), лекувани с GLP-1 рецепторни агонисти, са наблюдавани C-клетъчни карциноми на щитовидната жлеза. Тази зависимост не е потвърдена при хора, но семаглутид е противопоказан при пациенти с медуларен карцином на щитовидната жлеза или МЕН 2 (множествена ендокринна неоплазия тип 2) в анамнезата [4].
- Загуба на зрение при диабетици: при пациенти с диабет и предшестваща ретинопатия се препоръчва офталмологично наблюдение, особено при бързо подобряване на гликемичния контрол, на базата на данните от SUSTAIN-6 [7].
- Загуба на зрение при недиабетици:Освен това съществуват данни от ретроспективно кохортно проучване (включващо над 16 000 пациенти) че семаглутид и други GLP-1 агонисти имат връзка с повишен риск от неартериитна предна исхемична оптична невропатия (NAION) — състояние, при което се нарушава кръвоснабдяването на зрителния нерв, водещо до внезапна и безболезнена загуба на зрение. Кумулативната честота на заболяването за период от 3 години е 6.7% при приемащите семаглутид спрямо 0.8% при контролната група, като най-голям брой случаи се регистрират през първата година от лечението. Важно е да се отбележи, че макар относителният риск да е значително повишен, самото заболяване NAION в общата популация остава много рядко (среща се при около 2 до 10 на 100 000 души). Тъй като проучването е наблюдателно, то доказва само статистическа връзка. Точните рискови фактори все още не са изяснени [20].
Противопоказания
- Анамнеза за медуларен карцином на щитовидната жлеза или МЕН 2
- Свръхчувствителност към семаглутид или съставките на препарата
- Бременност (препоръчва се прекратяване минимум 2 месеца преди планирана бременност)
Съхранение на Семаглутид
Правилното съхранение на семаглутид е важно за запазване на неговата ефикасност.
Препоръки за съхранение:
- Неотворена писалка: съхранява се в хладилник при температура 2°C-8°C до изтичане на срока на годност.
- След първа употреба: може да се съхранява до 28 дни на стайна температура под 30°C.
- Да не се замразява. Ако препаратът е замразен, не трябва да се използва.
- Да се пази от пряка слънчева светлина.
- Да не се разклаща.
- Неотворени писалки, извадени от хладилник, могат да бъдат използвани в рамките на 28 дни, ако са съхранявани при температура под 30°C.
Скорошно регулаторно решение на EMA позволява транспортиране на инжекционен семаглутид при температури до 30°C за период до 48 часа — важно улеснение за пациенти, пътуващи или транспортиращи лекарството на по-голямо разстояние [1].
Как да си набавим Семаглутид за отслабване?
Истински семаглутид може да се набави само от аптечната мрежа, след като получите рецепта за него от квалифициран лекар.
Продуктите носещи етикет “семаглутид” които се продават в интернет НЕ са оригинални продукти и често пъти съдържат по-слабо ефективни пептиди, като например лираглутид.
Понякога е възможно изобщо да не съдържат активна съставка или тя да е напълно различна от написаната на етикета.
Продажбата, покупката и притежанието на подобни продукти, закупени онлайн, са незаконни и нарушават както българското законодателство, така и патентните права на Ново Нордиск.
Ако Ви е харесала статията, моля последвайте ме и в социалните мрежи:
Източници
- Meier JJ, Gallwitz B, Giorgino F. Editorial: Reviews and Novel Clinical Perspectives on Semaglutide: A GLP-1 Receptor Agonist With Both Injectable and Oral Formulations. Front Endocrinol (Lausanne). 2021 Sep 23;12:760153. doi: 10.3389/fendo.2021.760153. PMID: 34630338; PMCID: PMC8496444.
- Andersen A, Knop FK, Vilsbøll T. A Pharmacological and Clinical Overview of Oral Semaglutide for the Treatment of Type 2 Diabetes. Drugs. 2021 Jun;81(9):1003-1030. doi: 10.1007/s40265-021-01499-w. Epub 2021 May 8. PMID: 33964002; PMCID: PMC8217049.
- Guja C, Dănciulescu Miulescu R. Semaglutide-the “new kid on the block” in the field of glucagon-like peptide-1 receptor agonists? Ann Transl Med. 2017 Dec;5(23):475. doi: 10.21037/atm.2017.10.09. PMID: 29285508; PMCID: PMC5733318.
- Nauck MA, Quast DR, Wefers J, Meier JJ. GLP-1 receptor agonists in the treatment of type 2 diabetes – state-of-the-art. Mol Metab. 2021 Apr;46:101102. doi: 10.1016/j.molmet.2020.101102. Epub 2020 Oct 14. PMID: 33068776; PMCID: PMC8085572.
- Berra CC, Rossi MC, Mirani M, Ceccarelli Ceccarelli D, Romano C, Sassi L, Peretti E, Favacchio G, Pastore I, Folini L, Graziano G, Lunati ME, Solerte SB, Fiorina P. Real world effectiveness of subcutaneous semaglutide in type 2 diabetes: A retrospective, cohort study (Sema-MiDiab01). Front Endocrinol (Lausanne). 2023 Jan 18;13:1099451. doi: 10.3389/fendo.2022.1099451. PMID: 36743930; PMCID: PMC9889982.
- Frías JP, Auerbach P, Bajaj HS, Fukushima Y, Lingvay I, Macura S, Søndergaard AL, Tankova TI, Tentolouris N, Buse JB. Efficacy and safety of once-weekly semaglutide 2·0 mg versus 1·0 mg in patients with type 2 diabetes (SUSTAIN FORTE): a double-blind, randomised, phase 3B trial. Lancet Diabetes Endocrinol. 2021 Sep;9(9):563-574. doi: 10.1016/S2213-8587(21)00174-1. Epub 2021 Jul 21. PMID: 34293304.
- Marso SP, Bain SC, Consoli A, Eliaschewitz FG, Jódar E, Leiter LA, Lingvay I, Rosenstock J, Seufert J, Warren ML, Woo V, Hansen O, Holst AG, Pettersson J, Vilsbøll T; SUSTAIN-6 Investigators. Semaglutide and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med. 2016 Nov 10;375(19):1834-1844. doi: 10.1056/NEJMoa1607141. Epub 2016 Sep 15. PMID: 27633186.
- Perkovic V, Tuttle KR, Rossing P, Mahaffey KW, Mann JFE, Bakris G, Baeres FMM, Idorn T, Bosch-Traberg H, Lausvig NL, Pratley R; FLOW Trial Committees and Investigators. Effects of Semaglutide on Chronic Kidney Disease in Patients with Type 2 Diabetes. N Engl J Med. 2024 Jul 11;391(2):109-121. doi: 10.1056/NEJMoa2403347. Epub 2024 May 24. PMID: 38785209.
- Aroda VR, Bauer R, Christiansen E, Haluzík M, Kallenbach K, Montanya E, Rosenstock J, Meier JJ. Efficacy and safety of oral semaglutide by subgroups of patient characteristics in the PIONEER phase 3 programme. Diabetes Obes Metab. 2022 Jul;24(7):1338-1350. doi: 10.1111/dom.14710. Epub 2022 May 9. PMID: 35373893; PMCID: PMC9321749.
- Marx N, Deanfield JE, Mann JFE, Arechavaleta R, Bain SC, Bajaj HS, Bayer Tanggaard K, Birkenfeld AL, Buse JB, Davicevic-Elez Z, Desouza C, Emerson SS, Engelmann MDM, Hovingh GK, Inzucchi SE, Jhund PS, Mulvagh SL, Pop-Busui R, Poulter NR, Rasmussen S, Tu ST, McGuire DK; SOUL Study Group. Oral Semaglutide and Cardiovascular Outcomes in People With Type 2 Diabetes, According to SGLT2i Use: Prespecified Analyses of the SOUL Randomized Trial. Circulation. 2025 Jun 10;151(23):1639-1650. doi: 10.1161/CIRCULATIONAHA.125.074545. Epub 2025 Mar 29. PMID: 40156843; PMCID: PMC12144549.
- Wilding JPH, Batterham RL, Calanna S, Davies M, Van Gaal LF, Lingvay I, McGowan BM, Rosenstock J, Tran MTD, Wadden TA, Wharton S, Yokote K, Zeuthen N, Kushner RF; STEP 1 Study Group. Once-Weekly Semaglutide in Adults with Overweight or Obesity. N Engl J Med. 2021 Mar 18;384(11):989-1002. doi: 10.1056/NEJMoa2032183. Epub 2021 Feb 10. PMID: 33567185.
- Davies M, Færch L, Jeppesen OK, Pakseresht A, Pedersen SD, Perreault L, Rosenstock J, Shimomura I, Viljoen A, Wadden TA, Lingvay I; STEP 2 Study Group. Semaglutide 2·4 mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, double-dummy, placebo-controlled, phase 3 trial. Lancet. 2021 Mar 13;397(10278):971-984. doi: 10.1016/S0140-6736(21)00213-0. Epub 2021 Mar 2. PMID: 33667417.
- Rubino D, Abrahamsson N, Davies M, Hesse D, Greenway FL, Jensen C, Lingvay I, Mosenzon O, Rosenstock J, Rubio MA, Rudofsky G, Tadayon S, Wadden TA, Dicker D; STEP 4 Investigators. Effect of Continued Weekly Subcutaneous Semaglutide vs Placebo on Weight Loss Maintenance in Adults With Overweight or Obesity: The STEP 4 Randomized Clinical Trial. JAMA. 2021 Apr 13;325(14):1414-1425. doi: 10.1001/jama.2021.3224. PMID: 33755728; PMCID: PMC7988425.
- Garvey WT, Batterham RL, Bhatta M, Buscemi S, Christensen LN, Frias JP, Jódar E, Kandler K, Rigas G, Wadden TA, Wharton S; STEP 5 Study Group. Two-year effects of semaglutide in adults with overweight or obesity: the STEP 5 trial. Nat Med. 2022 Oct;28(10):2083-2091. doi: 10.1038/s41591-022-02026-4. Epub 2022 Oct 10. PMID: 36216945; PMCID: PMC9556320.
- Knop FK, Aroda VR, do Vale RD, Holst-Hansen T, Laursen PN, Rosenstock J, Rubino DM, Garvey WT; OASIS 1 Investigators. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2023 Aug 26;402(10403):705-719. doi: 10.1016/S0140-6736(23)01185-6. Epub 2023 Jun 26. PMID: 37385278.
- Wharton S, Lingvay I, Bogdanski P, Duque do Vale R, Jacob S, Karlsson T, Shaji C, Rubino D, Garvey WT; OASIS 4 Study Group. Oral Semaglutide at a Dose of 25 mg in Adults with Overweight or Obesity. N Engl J Med. 2025 Sep 18;393(11):1077-1087. doi: 10.1056/NEJMoa2500969. PMID: 40934115.
- Lincoff AM, Brown-Frandsen K, Colhoun HM, Deanfield J, Emerson SS, Esbjerg S, Hardt-Lindberg S, Hovingh GK, Kahn SE, Kushner RF, Lingvay I, Oral TK, Michelsen MM, Plutzky J, Tornøe CW, Ryan DH; SELECT Trial Investigators. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med. 2023 Dec 14;389(24):2221-2232. doi: 10.1056/NEJMoa2307563. Epub 2023 Nov 11. PMID: 37952131.
- Sanyal AJ, Newsome PN, Kliers I, Østergaard LH, Long MT, Kjær MS, Cali AMG, Bugianesi E, Rinella ME, Roden M, Ratziu V; ESSENCE Study Group. Phase 3 Trial of Semaglutide in Metabolic Dysfunction-Associated Steatohepatitis. N Engl J Med. 2025 Jun 5;392(21):2089-2099. doi: 10.1056/NEJMoa2413258. Epub 2025 Apr 30. PMID: 40305708.
- Rivera FB, Arias-Aguirre E, Aguirre Z, Ybañez MJC, Rubia JMM, Galang DJ, Lumbang GN, Ruyeras JMMJ, Magalong JV, Pine PL, Amigo JAC, Ansay MFM, Zelenkov N, Thomas SS, Vijayaraghavan K. Evaluating the safety profile of semaglutide: an updated meta-analysis. Curr Med Res Opin. 2024 Sep;40(9):1495-1514. doi: 10.1080/03007995.2024.2383731. Epub 2024 Jul 27. PMID: 39046272.
- Hathaway JT, Shah MP, Hathaway DB, Zekavat SM, Krasniqi D, Gittinger JW Jr, Cestari D, Mallery R, Abbasi B, Bouffard M, Chwalisz BK, Estrela T, Rizzo JF 3rd. Risk of Nonarteritic Anterior Ischemic Optic Neuropathy in Patients Prescribed Semaglutide. JAMA Ophthalmol. 2024 Aug 1;142(8):732-739. doi: 10.1001/jamaophthalmol.2024.2296. PMID: 38958939; PMCID: PMC11223051.